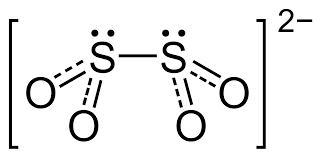
para que atomos de enxofre e potassio adquiram configuração eletronica igual a de um gas nobre e necessario que:
Respostas
1
O que é o teorema do octeto?
O teorema do octeto afirma que, para ser estável, um átomo de um elemento deve ter oito elétrons em sua camada de valência, a fim de obter o arranjo eletrônico do gás nobre.
Como:
O enxofre tem 16 elétrons e a configuração eletrônica do estado fundamental do arranjo da camada eletrônica é 2 – 8 – 6. Portanto, o átomo tem 6 elétrons de valência e precisa adquirir mais 2 elétrons para ficar estável.
O potássio tem 19 elétrons e arranjo de elétrons no estado fundamental com arranjo de elétrons da camada: 2 – 8 – 8 – 1. Assim, para ser uma camada, há 1 elétron na camada de valência, mas 8 elétrons na camada. A valência então perde esse elétron. ,
Portanto, para que o átomo de enxofre e o átomo de potássio tenham o mesmo arranjo eletrônico que o gás nobre, o enxofre deve doar dois elétrons e o potássio deve doar um elétron.
————————————————————————————————————————
2
Resposta: O enxofre ceda 2 elétrons e que o potássio ceda 1 elétron.