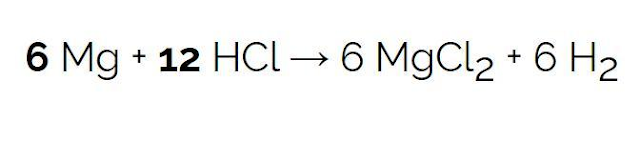Considerando-se a equação química não balanceadaMg + HCl → MgCl2 + H2
e admitindo-se, num balanceamento, o coeficiente 6 (seis) para cada produto, o coeficiente de cada reagente será, respectivamente:
b) 6 e 6.
c) 6 e 12.
d) 12 e 6.
e) 12 e 12.
Respostas
1
Considere a equação estequiométrica Mg + HCl → MgCl2 + H2 e suponha que no equilíbrio os coeficientes de cada produto são 6 (6) e os coeficientes de cada reagente são c) 6 e 12.
Para determinar os coeficientes de cada reagente, sabendo que um fator de 6 para cada produto é aceitável para equilibrar a equação química, devemos primeiro colorir cada produto e depois multiplicar a base do reagente pelo coeficiente.
Mg + HCl → 6 MgCl 2 + 6 HCl
Então temos 6 átomos de magnésio (Mg), então o coeficiente reagente é:
6 mg + HCl → 6 mg cada 2 + 6 HCl
Agora, multiplicando a potência de 2 pelo multiplicador de 6 dá ao reagente o coeficiente de HCl 12 porque há 12 átomos de cloro (Cl) e 12 átomos de hidrogênio (H) no produto.
6 mg + 12 HCl → 6 mg cloreto 2 + 6 HCl
———————————————————————————————————————-
2
Mg-6 —-> Mg-6
CL-12 ——-> CL-12
H-12 ——–> H-12
espero que isso seja útil